11月5日,中國科學(xué)院上海營養(yǎng)與健康研究所邵振研究組在Nature Communications發(fā)表研究論文:Transcription factor ZNF263 primes human embryonic stem cells for pluripotency dissolution and lineage commitment。該研究結(jié)合大規(guī)模計算生物學(xué)篩選分析和一系列功能實驗,揭示了鋅指轉(zhuǎn)錄因子ZNF263在調(diào)控人胚胎干細(xì)胞始發(fā)多能態(tài)建立維持、多能性融解直至胚層分化命運決定這一連續(xù)動態(tài)過程中的關(guān)鍵作用。
研究人員首先搜集了大量不同人類細(xì)胞類型和狀態(tài)的表觀基因組數(shù)據(jù),并應(yīng)用前期開發(fā)的MAmotif工具包進(jìn)行大規(guī)模計算生物學(xué)篩選,發(fā)現(xiàn)ZNF263結(jié)合motif顯著富集在始發(fā)態(tài)人胚胎干細(xì)胞中特異性激活的基因啟動子上,暗示它很可能在人類多能性調(diào)控網(wǎng)絡(luò)中扮演某種重要角色。
然后,研究人員通過ChIP-seq實驗證實,ZNF263在人胚胎干細(xì)胞中廣泛結(jié)合多能性維持和干細(xì)胞分化相關(guān)基因的啟動子,形成一個獨立于POU5F1(OCT4)、SOX2和NANOG等核心多能性因子的調(diào)控模塊,暗示它可能有不同的多能性調(diào)控作用。研究團(tuán)隊進(jìn)一步構(gòu)建了ZNF263敲除的人胚胎干細(xì)胞系,發(fā)現(xiàn)ZNF263缺失后,堿性磷酸酶活性等多能性標(biāo)志物和PRDM14等原始多能態(tài)相關(guān)基因表達(dá)上調(diào),而ZIC2等早期分化因子表達(dá)下調(diào),暗示始發(fā)多能態(tài)相關(guān)的基因表達(dá)平衡受到破壞。更深入的機(jī)制分析表明,在人胚胎干細(xì)胞中,ZNF263通過直接調(diào)控ZIC2的表達(dá)和染色質(zhì)結(jié)合,進(jìn)而建立以ZNF263-ZIC2軸為核心的正前饋回路,驅(qū)動基因表達(dá)程序從多能性維持向譜系分化偏移,使細(xì)胞為多能性退出和胚層分化命運決定做好準(zhǔn)備。
最后,研究人員指出ZNF263缺失后,人胚胎干細(xì)胞多能性退出過程的效率顯著降低,向三個胚層特別是外胚層分化的能力受到明顯損害。單細(xì)胞轉(zhuǎn)錄組分析則指出,野生型始發(fā)態(tài)人胚胎干細(xì)胞中,存在兩個分別表現(xiàn)出較高中內(nèi)胚層和外胚層分化傾向的細(xì)胞亞群;而ZNF263缺失后,這些高譜系分化傾向的細(xì)胞比例顯著降低。
上述研究系統(tǒng)揭示了ZNF263在人胚胎干細(xì)胞中,通過調(diào)控多能性維持與譜系分化兩方面基因之間的表達(dá)平衡,主導(dǎo)了始發(fā)多能態(tài)基因表達(dá)程序的建立和維持,并進(jìn)一步助推后續(xù)多能性退出和胚層分化過程。其與ZIC2等早期發(fā)育因子之間的協(xié)同作用以及與Wnt等關(guān)鍵發(fā)育信號通路的互作,有可能為進(jìn)一步理解人類細(xì)胞多能性狀態(tài)轉(zhuǎn)換和早期胚胎發(fā)育的分子調(diào)控機(jī)制提供新的線索。
營養(yǎng)與健康所副研究員尹倩倩、博士后黃靜、博士畢業(yè)生孫洪鐸、研究生周書晗為該論文共同第一作者,研究員邵振為通訊作者。該研究受到國家科技部、國家自然科學(xué)基金委員會、中國科學(xué)院等基金的資助。
論文鏈接:https://www.nature.com/articles/s41467-025-64290-5
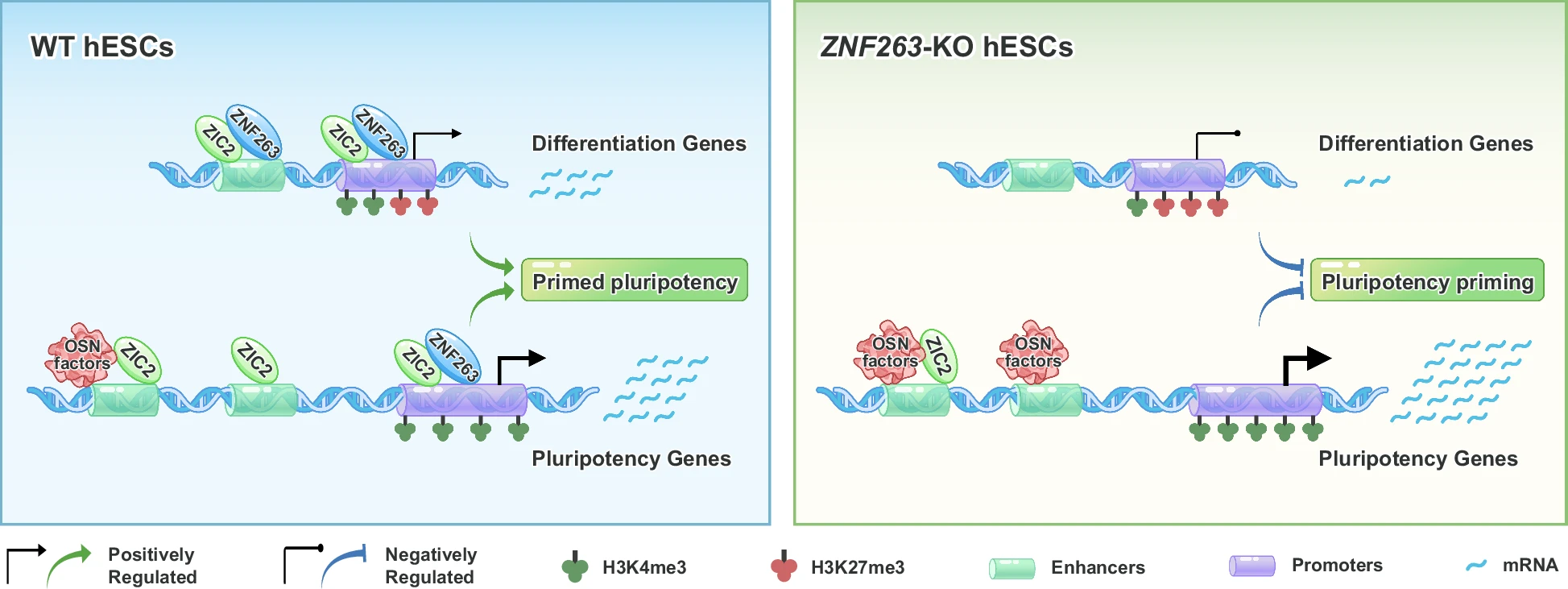
圖:在人胚胎干細(xì)胞中,ZNF263通過以ZNF263-ZIC2軸為核心的正前饋回路,驅(qū)動了始發(fā)多能態(tài)轉(zhuǎn)錄程序的建立
推送單元:邵振研究組、科技規(guī)劃與任務(wù)處